死神使者:癌症

本文转自微信公众号:老和山下的小学僧(ID:gh_586564bb7b66),封面:unsplash
我们离癌症有多远?
国家癌症中心数据显示,一个人从40岁开始,患癌概率显著上升,活到74岁,累积患癌率21%,活到85岁,累积患癌率36%。可以说,如果一个人没有因其他原因死亡,那么到头来有三分之一的可能就是癌症。

这有多可怕?一家三口加双方父母共7口人,终其一生,7人全都不患癌症的概率是4.4%,双方父母四人,活到74岁全都不患癌症的概率是39%。如果再把亲戚朋友算上,几乎没有多少家庭能躲开癌症。
我们与癌症近在咫尺!
所以,了解癌症很有必要,最大的致癌因素是什么?估计你八成会猜错。
了解癌症有哪些渠道?肯定不是商家医院的广告。
治疗癌症有哪些方法?大多数人的认知停留在二十年前。
哪些癌症已经能治愈?你可能认为这是天方夜谭。
不急,从头说起。
不靠谱的化学反应
癌症来自基因突变,即DNA出错。在最理想状况下,DNA复制转录出错的概率是十亿分之一,这是人体衰败的主因,也是人类进化的根源。
这十亿分之一的概率能不能消除?
从硬件上说,人体的本质是一堆化学反应,化学反应的本质是原子外层电子的相互作用,量子力学告诉我们,电子的本质是个不靠谱的家伙,它的行为只能用概率描述。因此,要把化学反应的出错率降到零,是不可能的。
这十亿分之一的概率会不会增加?
影响化学反应实在是一件很容易的事情,但凡能引起DNA出错的东西,都叫致癌物。判断一个东西是否致癌并不轻松,除了那些权威机构公布的不知有多少可信度的致癌物清单之外,我们不妨从癌症统计数据中再找些规律。
推荐国家癌症中心每年发布的全国癌症统计报告,值得专门撰文解读,不过咱这儿就简单从2019年1月发布的报告里摘几个结论:
-
城市发病率高于农村
-
农村死亡率高于城市
-
城市农村癌症种类差异明显
-
男性发病率排第一,肺癌
-
女性发病率排第一,乳腺癌
-
男女死亡率排第一,肺癌
该注意啥,心里有点数了没?像医学养生这类知识,对于外行来说,去看微观研究,不如看宏观统计。这份报告蕴藏的信息量非常大,建议全篇背诵。
还有一份美国癌症学会出的全球癌症统计报告,学术价值更大一点,建议全篇略读。不过,这里有个结论估计能让人大跌眼镜。
你猜猜,全球癌症发病率最高的国家都有哪些?丹麦、挪威、法国、新西兰、比利时……一水儿的发达国家,而中国的癌症发病率远低于日本德国,没想到吧?
这是为何?原因无他,就是活得太长了,人均寿命排行榜和癌症发病率排行榜如出一辙。虽然有些穷国家的统计很粗糙,但不影响这个基本结论。
当然也有例外,日本人均寿命排第一,但癌症发病率只有40名左右;美国人均寿命第30-40名,但癌症发病率有望杀入十强;中国人均寿命大约50名,癌症发病率大约80名。不过,咱这两个排名都在显著增加,不知是该高兴还是悲伤……
媒体老是拿“癌症发病率上升”这事来证明环境污染越来越严重,但搞笑的是,这其实是迈向发达国家的标志。根据国家癌症中心的结论,中国癌症发病率的增加主要由寿命增加引起,标化发病率水平基本持平,同一年龄段的癌症发病率并没有增加。
以上内容都是引用,别和我争,下面才是个人观点:人均寿命和癌症发病率相结合,可以作为食品安全与环境污染的评价指标,这方面,中国比预想中好很多,至少没有继续恶化,甚至还有好转的趋势,或许还能媲美普通发达国家。
癌症死亡率则是评价整体医疗水平的关键指标,这方面,中国与发达国家差距甚大,60%的癌症患者活不过5年,而发达国家的这一数据只有20%-40%,十年前的中国是70%。
细胞涅槃
回到微观,癌症到底是个什么东西?
人体大约50万亿个细胞,都从一个受精卵分裂而来。受精卵在刚开始阶段,一分二、二分四、四分八……这德性和癌细胞没什么两样。

斑马鱼受精卵分裂过程,视频时长20小时
但从某个时间开始,这种无限分裂的开关被关了,细胞分化出不同类型,神经细胞、皮肤细胞、肌肉细胞等等,这些细胞有个共同点,寿命一到就得死亡(暂不论生殖细胞)。
操纵这一切的,就是基因。
基因不断突变,只要凑巧把这个开关打开了,细胞就会重启无限分裂的技能,这种细胞其实和正常细胞差别不大,只是它没有寿命限制,会无限分裂,最终靠数量把人体压垮。
说到底,癌细胞就是追求长生不老的正常细胞,并且它成功了。
不过暂时还不用怕,咱有免疫系统。
癌细胞出现后,会和免疫系统上演一场“适者生存”的戏码。其实正常人每天都会产生不少癌细胞,毕竟咱有十亿分之一的突变概率嘛,只不过它们都会被免疫系统清除。各位,给免疫系统的功劳簿上再记一笔吧!

T细胞杀死癌细胞,视频时长40分钟
但免疫系统并不是一块铁板,漏洞也就比筛子少一点,无数前仆后继的癌细胞,只要撞上了漏洞,就能发展成癌症,所以癌症种类非常多。
这还没完,能躲过免疫系统追杀的癌细胞,基因突变概率往往特别高,从十亿分之一提高到百万分之一也是等闲。于是,更快的分裂速度,更高的突变概率,使得癌细胞进化速度暴增,不但把免疫系统打成了筛子,对药物也具备很强的抵抗力。
更恐怖的是,癌细胞还能进化出组织能力,可以派侦察兵寻找好地方并潜伏下来,一旦主基地被毁,就可以发展第二基地。
操纵这一切的,也是基因。
把癌细胞在人体内的演化,看成生命在地球上的演化,就不会惊讶于癌细胞表现得像智慧生物。
对我们人来说,每次基因突变,就是一场赌局,只要赌的时间足够长,总有输的一天。俗话说得好,哥来到这个世界上,就没打算活着回去。
癌症能根治吗?
抬个杠,什么叫治疗?
仍以感冒为例。感冒由病毒引起,治疗就是杀病毒,病毒是被免疫系统杀死的。那么问题来了,协助免疫系统更快更好地杀病毒,算不算治疗?比如喝水,比如吃饭,又或者是某些特殊的尚不明确的化学物质,比如中药。这个话题放一边。
再抬个杠,什么叫根治?
如果把癌细胞杀的一个不剩叫根治,那就别想了,即便正常人每天都会产生癌细胞。如果把发展成癌症的那类癌细胞杀光了叫根治,那也很麻烦,因为癌细胞一直在变异,你甚至都分不清,新癌细胞是从正常细胞变异来的,还是从老癌细胞变异来的。如果癌症治愈后10年再得癌症,10年前那次治疗算根治吗?
不抬杠了,癌症一般不叫根治,而叫:5年生存率。
患者在治疗后,即便用最先进的检测技术证明所有参数都正常了,医生也不敢说根治,至少要等一段时间再说,要等多久呢?
5年!
这个5年有什么深刻机理吗?不好意思,只是个统计数据而已:3年不复发,80%的可能是治愈了;5年不复发,90%的可能是治愈了;抱歉,这个世界没有100%的事情。
一般认为,患者在5年内没有复发,就算治愈了。

中学生物知识复习的差不多了,下面说些作为一个成年人应该知道的东西。
本僧先把个人观点亮这儿:把人类与癌症的对抗看成一场持久战的话,现在至少是战略相持阶段。人类的抗争,已经从小米加步枪的战斗,一路成长到海陆空天全方位的高科技战争。
这是一部精彩绝伦的战争大片!
无差别攻击
大多数人对癌症的印象就是:切除+放疗/化疗,然后等死。
这显然是极大的误解,放化疗对人体细胞算是无差别攻击,虽是无奈之举,但也没有那么不堪。
普通战斗
如果癌细胞没有扩散,而且长在能切的部位,那么切除确实是最好的办法,治愈率非常高,说十拿九稳也不夸张。
老生常谈:治疗癌症,早发现最重要。
但是,癌细胞组织特别松散,很容易脱落,若遇到庸医,把肿瘤弄破了,哪怕只是逃出去几个癌细胞,很可能就会东山再起。1克的肿瘤团块,就有10亿个癌细胞,掉下一丁点,妥妥就少半条命。
最麻烦的是,目前任何技术,都无法检测出体内残存的少量癌细胞,更分不出这是手术后残留的,还是手术前扩散的,都得等上三五年再说。因此,找个好医生动刀很有必要。
这儿又有一个让你意向不到的事情:单就手术开刀这个环节,中国医生的水平是全球顶级的,原因无他,唯手熟尔。
对中国医生来说,日均1例手术都不叫个事,一年手术量够国外医生做一辈子了。

手术量大的医院,手艺都不会太差
局部战役
如果没法手术或者担心手术后有残留,并且癌细胞祸害的区域仍在局部,就可以考虑放疗(化学药物治疗叫化疗,放射性治疗叫放疗)。
传统放疗一般用伽马射线之类的,这玩意儿简直就是机枪扫射,不管好人坏人,鸡犬不留,而且放射线本身也是一种致癌物,会增加正常DNA出错的概率,副作用贼大。
为了减少副作用,最近几年科学家正在尝试用质子束进行放疗,就是所谓的“质子疗法”,也是放疗的一种。
虽然这技术前景尚不明朗,目前也没有表现出更出色的疗效,但就是贵,原因你懂的。
全面战争
如果癌细胞扩散全身或者白血病这类非实体肿瘤,通常就得化疗。
用化学药治疗的逻辑是,先找到癌细胞和正常细胞的区别,再开发相应的化学药物。但癌细胞源自正常细胞,两者差别不大,早些年,科学家只知道癌细胞比正常细胞分裂速度更快。无奈,只能拿这个做文章。
早期的化疗药不管正常细胞和癌细胞,只是粗暴地抑制所有细胞的分裂速度。这下就炸锅了,看看正常细胞的更新周期:肠细胞2-5天,皮肤细胞28天,白细胞2-3周,红细胞4个月,肝细胞5个月……只有神经细胞、心肌细胞等少数细胞是一辈子不更新的。
化疗药这么蛮干,虽然对抑制癌细胞很有效,但也对人体产生了系统性的负面影响!最显眼的就是,分裂旺盛的头发被长期抑制后,患者大多成了光头。
可即便是“两害相权取其轻”的妥协方案,依然耗费了无数人的心血。

认识这植物嘛?太平洋紫杉,红豆杉的一种,从紫衫树皮中提取的“紫杉醇”,号称抗癌第一药。科学家花了20年,测试了3万个样本,才找到这个迄今为止最优秀的天然抗癌药。
了解其抗癌原理要懂些高中生物知识,简单来说,紫杉醇会让微管蛋白聚成一团,抑制纺锤体形成,破坏有丝分裂,导致细胞分裂卡在DNA合成后期无法继续。
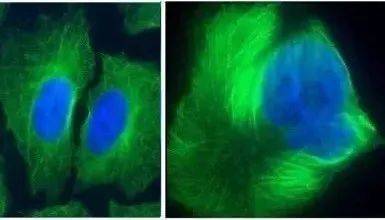
左边细胞顺利分裂成2个,右边微管蛋白被紫杉醇搅成一团,细胞分裂被冻结。
紫杉醇一经问世便疗效斐然,甚至对复发性卵巢癌的有效率都达到了30%!这在上世纪80年代是爆炸性事件,要不是环保组织拦着,紫衫差点被砍到绝种。(认真点,这不是玩笑!)
到底是什么化学物质如此神奇?来,给你看一眼:

这儿有个严肃的事情,很多人不问原理,只听说红豆杉能抗癌,就把它当成防癌补品来用。如果抗癌和防癌是一回事,那子弹就可以当防弹衣用了。当他们知道紫杉醇是抑制细胞分裂的化疗药,正常人吃了和吃毒药差不多的时候,不知道是个啥表情?

顺便捅一下马蜂窝,你说,这玩意儿算中药吗?算中药治疗癌症的例证吗?
如果还嫌不够热闹的话,再捅几下:从秋水仙提取的秋水仙碱,从长春花提取的长春花碱,从美登木提取的美登木素,都是通过抑制微管蛋白的聚合(紫杉醇是让微管蛋白过分聚合),破坏纺锤体成形,最终让细胞分裂停止。
虽然长春花、美登木很早就是一味药材了,在传统医学里使用颇多,但发现其抗癌成分的是美国人和加拿大人。从确定疗效到确定成分,再到提纯,再到人工合成,再到改进配方,所费心血不知凡几。
举个例子,法国科学家Potier在用10-DAB合成紫杉醇的过程中,发现一个中间产物叫RP5676,比紫杉醇更能结合微管蛋白,后来这个中间产物就成了新的抗癌药:多西他赛。
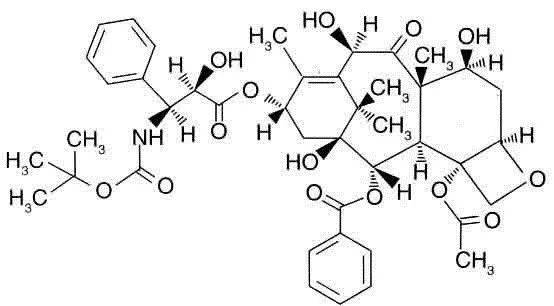
不说中药话题了,本僧怕外行的口水。
手术、放疗、化疗是癌症治疗三大利器,三者往往结合使用,有些局部治疗也用化疗,有些全身治疗也用放疗。虽然是无差别攻击,但只要治疗得当,三大利器对付癌症还是很有效的。
不过癌症治疗是极其复杂的工作,不然IBM花了几百亿的Watson系统也不会铩羽而归,所以没法指望每个医生都能制定完美的治疗方案。
治疗得当是幸运,治疗失当也不稀奇。
心理战
信息时代的坏处是人人都知道放疗化疗的副作用,这种心理暗示在治疗过程中造成的伤害不容小觑。如果再遇到一个庸医,那治疗就和催命没啥区别了!
原本免疫系统在和癌细胞的攻防战中还能勉强维持,放化疗一顿瞎搞,杀敌八百自损一千。可人家癌细胞恢复力强啊,等它们缓过劲发动第二波攻势,就剩摧枯拉朽了。
听过很多医生感慨说:癌症死亡有三分之一是被吓死的,还有三分之一是治疗不当,最后三分之一才是真正无力回天。当然,感慨只是感慨,当不得真。
再一句老生常谈:好心态和好医生同样重要!
小结:作为一个合格的成年人,应该要知道,大部分早期癌症完全可以通过手术治愈;情况稍微严重点,加上放化疗还是能轻松控制,甚至治愈;只有严重的癌症,才不得不听天由命。
精确打击
幸运的是,到了21世纪,癌症治疗开始不再是简单粗暴的无差别攻击,而是寻找癌细胞和正常细胞之间更多的不同点,这就是“靶向药”的概念。
让我们通过人类第一个靶向药的研发,来领略一下科技的风采吧!
1959年美国费城有2位研究员,意外发现慢粒白血病患者的22号染色体特别短小,这一发现冲击了“癌症由病毒引起”的主流观点,医学界立马沸腾了。
22号染色体消失的部分去了哪里?13年后,芝加哥的科学家发现了慢粒白血病患者另一条异常染色体:9号染色体变长了。
到了这会,就是我们这些外行也能猜到:两条染色体断裂后形成易位,22号染色体的长臂,跑到了9号染色体上。科学家很快证实了这一点,并称之为费城染色体。

俩染色体易位有什么后果?又过了13年,科学家发现,9号染色体断点的ABL基因编码是一种促进细胞分裂的激酶,这种激酶是保证正常细胞分裂所需的,活性会受到严格控制。但ABL基因和22号染色体断点的BCR基因结合之后,使得激酶像电脑程序卡死一样,始终处于高活性状态,导致细胞分裂失控,最终引起癌症。
科学家给这个发疯的激酶取了个名字,BCR-ABL蛋白。只要把BCR-ABL注入小白鼠体内,小白鼠就会有白血病症状。经过反复实验,最终证实,BCR-ABL正是造成慢性粒细胞白血病的原因。
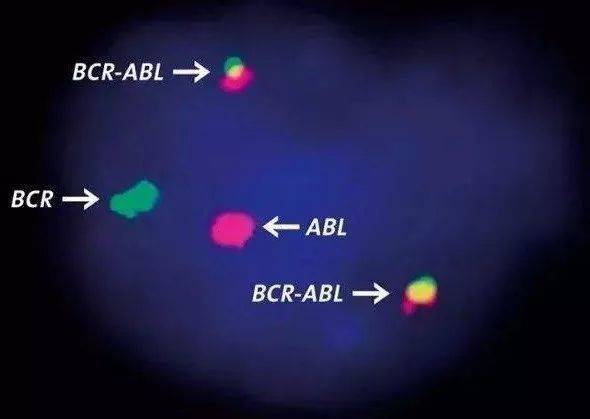
靶子终于找到了,接着就是打靶了。
医药公司这个时候才会介入,开始烧钱研发,可即便如此,也足足烧了15年,研究人员不断设计和修饰药物分子,最终开发出4-[(4-甲基-1-哌嗪)甲基]-N-[4-甲基-3-[[4-(3-吡啶)-2-嘧啶]氨基]苯基] -苯胺甲磺酸盐,光看名字就知道开发这玩意儿有多难了!
这种全新的化学成分学名甲磺酸伊马替尼,商品名:格列卫。它可以抑制BCR-ABL蛋白的活性点,对慢粒白血病有奇迹般的效果,而正常细胞没有这种蛋白,所以副作用非常有限。
有趣的是,这玩意儿不像紫杉醇是“纯天然提取的绿色产品”,而是人为设计并合成的新化学成分。但论副作用,能把纯天然的紫杉醇甩开几条街。本僧多嘴一句,纯天然和健康完全是两码事,本质还是要看里面的化学反应,别忘了,古代毒药基本都是纯天然的。
格列卫于2001年5月通过FDA批准,整个审批过程不到三个月,创造了FDA审批药物的最快记录,并评为当年的十大科技突破,是人类抗癌历史的里程碑。
格列卫凭借一己之力,将原本是绝症的慢粒白血病变成了类似高血压这样的慢性病,五年生存率超过90%!只要定期吃药,日常生活和普通人没两样,寿命也有保障,是目前最成功的靶向药。
更为欣喜的是,格列卫虽然不能直接让错位的染色体恢复正常,但给了人体系统充足的备战时间,最终大约有30%-40%患者的费城染色体转为阴性。

捋一下思路:发现癌细胞机理—人为设计药物分子—解决癌症,这套路看着无比痛快,但想到研发投入就无比痛心了!若是有些捷径,自然不应客气。
急性早幼粒细胞白血病,17号染色体和15号染色体易位,17号染色体上的RARα基因与15号染色体的PML基因形成PML-RARα融合基因,导致早幼粒细胞分裂不受控制,引发白血病。
这曾是一种极为凶险的白血病,几个月便可夺人性命!但现在用全反式维甲酸和三氧化二砷(砒霜)进行联合靶向治疗,五年生存率已超过90%,达到基本“治愈”标准。
这一治疗方案的灵感来源于一个民间中医的偏方,后来科学家从分子机理上揭示了诱导白血病细胞分化凋亡的过程,把疗效随缘的偏方升级成十拿九稳的抗癌药,中国前卫生部部长陈竺是这一成果的重要贡献者。

靶点
打蛇打七寸,慢粒白血病的BCR-ABL,急性早幼粒白血病的PML-RARα,就是癌细胞的七寸,医学上称之为“靶点”。只要找到了靶点,人类就很有希望制服癌症这条毒蛇。
但并非每一个靶向药都有格列卫这般神奇,或者说,几乎没有什么靶向药能全面超越格列卫。一般靶向药能把晚期五年生存率提高到30%就算很优秀了,因为其他癌细胞并没有像BCR-ABL这么容易搞定的特征靶点。
那咋办?科学家很快搬出了新武器。
美国科学家从癌细胞分泌物里发现了血管内皮生长因子VEGF,这是一种可以促进血管形成的蛋白。要知道,癌细胞的高效分裂是以消耗大量营养为代价的,而营养靠血管运送,所以肿瘤为了保证营养,会疯狂促进周边血管的生长。
于是,科学家提出了一种针对肿瘤血管,而不是针对癌细胞的治疗思路,靶点正是VEGF。
2004年美国FDA批准了第一个抗肿瘤血管生成药物,安维汀。它可以阻止VEGF与血管内皮细胞结合,抑制血管形成,大幅度削减了肿瘤的营养供应,从而抑制肿瘤生长和扩散转移,延长患者寿命。
不过,癌细胞勒紧裤腰带,日子还是能过的,有啥办法能彻底“饿死”癌细胞?
2018年1月《自然》的一篇文章让我们看到了希望,科学家发现了一种可以控制细胞内脂肪合成和营养物质循环再生的蛋白:REV-ERB。如果REV-ERB维持在较低水平,细胞就会允许合成脂肪并且把一些废弃的营养物质循环再生,如果REV-ERB的水平升高,细胞就会停止那些工作。这是一个正常操作,和人体生物钟有关。
癌细胞因为要合成营养,就得把REV-ERB的活性降到很低。科学家尝试激活了这个蛋白,结果发现,大量癌细胞真的被饿死了!更惊喜的是,正常细胞的REV-ERB活跃度本身就很高,所以在治疗过程中基本不受影响。
简单来说,癌细胞每天要吃10碗饭,正常细胞每天只吃1碗饭,科学家想办法把米饭供应降到了1碗,于是,癌细胞饿死了。哎,吃货到了哪里都不容易啊!
可惜,针对REV-ERB靶点的研究尚未成熟,靶向药更是无从谈起。

我猜你肯定很想知道,人类已经找到了多少靶点?又有多少已经开发出了靶向药?热爱祖国的同学可能还会多问一句:咱们国家做了多少贡献?
截止2018年底,从FDA批准的靶向药来看,已经开发出靶向药的靶点有:肺癌12个,乳腺癌6个,结直肠癌12个,白血病15个,淋巴瘤9个,甲状腺癌15个,黑色素瘤5个,肾癌27个,肝癌9个,胃癌3个,多发性骨髓瘤4个,胰腺癌7个……大伙自个上FDA官网和美国国家癌症研究院去数吧,若周边有人患了这类已经找到靶点的癌症,那也算不幸中的万幸了。
关于这数据有几个说明:
第一,本僧老眼昏花,若统计有误,真实数据只多不少。
第二,同一个靶点,不同医药公司会开发出不同药物,比如,已批准上市的针对EGFR靶点的药物至少有20个。
第三,不同癌症可能是同一个靶点。比如,7号染色体短臂上的表皮生长因子受体EGFR基因,与细胞增殖和信号传导密切相关,这个基因很容易突变(可能是杀人最多的基因了),一旦变成活跃状态,就会导致细胞分裂不受控制,引发癌症。这事若发生在肺部,就是肺癌,若发生在胰腺,就是胰腺癌。所以癌症按照部位分类并不是很精准。
第四,新的靶点仍不断被发现。举个例子,德克萨斯大学和上海交通大学的联合团队发现了急性骨髓性白血病的一个新靶点:LILRB4,该成果发表于2018年10月《自然》杂志,仅仅只是半年前的事情。

看得出来,医学的核心技术并不是材料技术。虽然日本的整体医疗环境是最好的,但从技术创新讲,美帝仍然是一骑绝尘。中国虽然进步很快,但总体实力和美帝差距甚大。
癌细胞的反击
靶向药为特定癌细胞量身定做,这和破解密码差不多,开发成本极高,可一旦癌细胞更改了密码,那之前的工作就白费了。
事实上,总会有一些癌细胞能抗住靶向药的攻击,因为癌细胞可以躲到几乎任何地方,而药物却不可能在每个地方都达到足够杀死癌细胞的浓度,于是,癌细胞的耐药性就出现了。
癌细胞有两大依仗:更快的分裂速度、更高的突变概率,这本质上是加速了进化速度。如果继续用靶向药的思路去破解密码,代价会越来越大,到头来人类很可能就陷到了癌细胞的迷宫里。
以死亡数最高的肺癌为例,EGFR基因突变导致的非小细胞肺癌是最常见的一种肺癌。第一代靶向药很快问世了,2003年上市的易瑞沙,2004年上市的特罗凯,还有2011年上市的凯美纳。
其中,凯美纳是中国第一个小分子靶向药,当时被卫生部长陈竺誉为民生领域的“两弹一星”,是中国医药界一个不小的突破。

尽管是很了不起的事情,可患者在服用第一代肺癌药后,几乎全都出现了耐药性。短则几个月,长则几十个月,EGFR基因就出现了新的变异,密码一改,靶向药自然就没用了。
于是,2013年第二代肺癌药阿法替尼上市,这显然不是终点,2015年第三代肺癌药奥希替尼上市,但依然无法阻止EGFR基因的突变,现在第四代肺癌药也已经上路了,未来肯定还有第五代……
需要注意,第三代不见得比第一代先进,只是因为癌细胞不停更换密码,就需要用不同抗癌药去破解,至于到底该吃第几代,千万听医生的,不可自作主张。
按这路数走,很难追上癌细胞的步伐,咋办?毛主席教导我们,要让敌人陷入人民战争的汪洋大海中。
人类的第一次总攻
反思一下人类对抗癌症的思路,都是用药物直接攻击癌细胞,而忽略了人体最强的武器:免疫系统。
免疫系统一旦投入战斗,不会放过任何一个入侵者,这就是人民战争的汪洋大海。
思路是挺好,但现实不太友好。
免疫系统运行的复杂性堪比国家政府,各种细胞分工合作的精细程度让人咋舌,工程学告诉我们,越复杂的设备越容易出问题,免疫系统自然不会例外。
第一个漏洞
免疫系统的战斗原则一般是先识别再杀伤。如果免疫系统要对人体每一个细胞进行识别检查,那肯定得累死,咱们摄入的食物不足以支撑如此高能耗的行动。所以,人体细胞进化出了一种自我检查的能力,它们把检查结果通过一种叫MHC的分子展示在细胞表面。
这样一来,免疫系统的工作量就大大降低了,只要看一下细胞表面的MHC分子就算完成了日常检查。比如,如果有个细胞被病毒入侵了,那么它呈现的MHC分子就会有异常信号,T细胞就会赶来把这个异常细胞杀死,完事后再让吞噬细胞清理战场,让一切恢复如初。
再比如,正常细胞变成癌细胞后,呈现的MHC分子通常也会有异常信号,是的,“通常会有”,因为癌细胞疯狂分裂,一定会产生很多乱七八糟的蛋白,所以产生的MHC信号必然会变异常,一旦这个信号被放出去,T细胞大军就会赶来杀敌。
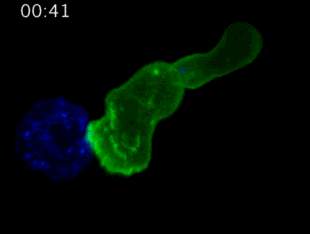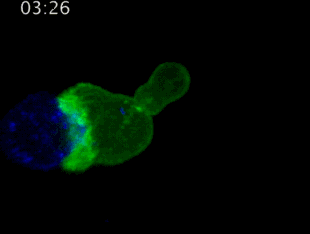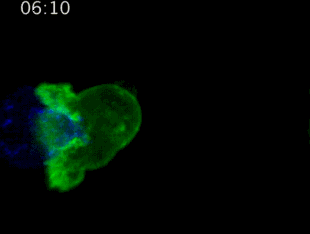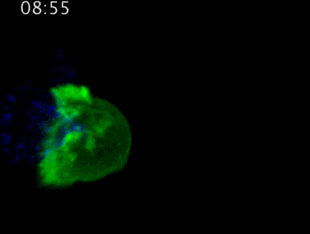
剑桥大学拍摄:T细胞(绿)冲向癌细胞(蓝)
癌细胞当然不会坐以待毙,在“不通常”的情况下,癌细胞会抑制MHC信号的呈现,只要不让MHC信号送到细胞外面,就能成功躲避免疫系统的检查,然后也就没T细胞啥事了。
我们姑且把这类癌细胞称为:不放信号的癌细胞。
第二个漏洞
除了这些胆小的癌细胞,还有一些胆大的癌细胞,它们敢于和T细胞正面硬抗。
T细胞因为杀伤力太强,稍有不慎就会对正常细胞造成误伤,所以免疫系统进化出了一套暗号系统,沿途的正常细胞通过和T细胞对暗号,避免被误伤。T细胞表面用来对暗号的蛋白,学名:免疫检查点。
正常细胞如果把暗号对错了,T细胞也会毫不留情出手,这就是免疫缺陷疾病,如,类风湿关节炎、红斑狼疮。
在成千上万的癌细胞中,也会有个别癌细胞蒙中暗号,躲过T细胞追杀。
我们姑且把这类癌细胞称为:能对暗号的癌细胞。
实力尚存的免疫细胞
总结来说,癌细胞通过这两个漏洞,只是躲过了免疫系统的检查和追杀,并不是在正面战场堂堂正正击败T细胞。换句话说,只要免疫系统堵住漏洞,那么T细胞杀死癌细胞依然和切菜一样容易。
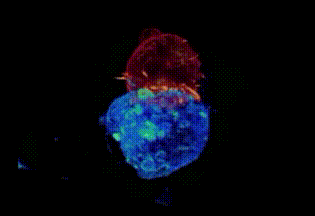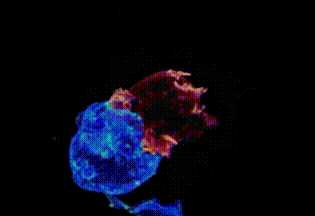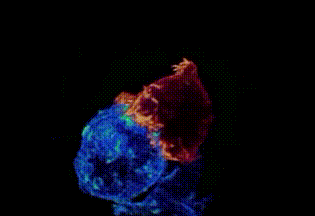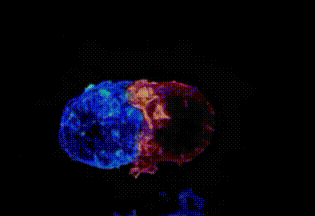
剑桥大学拍摄:T细胞(红)缠住癌细胞(蓝)搏斗,绿色是T细胞释放的毒素
这就是所谓的“免疫疗法”。
免疫疗法是人类第一次对癌症发起的总攻,意图彻底解决所有癌症,只是战事并没有那般顺利。不过,这个词已经被某某系医院玩坏了,被说成了包治百病的万能药,大家先把之前的信息清空,且听本僧从头道来。
第一个补丁
2018年诺贝尔医学奖颁给了美国的詹姆斯艾利森和日本的本庶佑,以表彰他们在癌症免疫疗法上做出的开创性工作。免疫疗法,是当年的十大科技突破之首。
艾莉森找到的CTLA-4蛋白是人类首个被发现的“免疫检查点”,也就是癌细胞和T细胞对的暗号。艾莉森提出了一种全新的对抗癌症思路,他设计了一种药物专门结合CTLA-4蛋白,破坏这个暗号系统,于是,T细胞就开始重新追杀癌细胞。
2011年FDA批准用于治疗晚期黑色素瘤的新药Yervoy,正是基于这个原理。

但事情很棘手,因为T细胞的CTLA-4蛋白被破坏,很多用CTLA-4暗号的正常细胞也被T细胞杀死了。很多患者得了严重的自身免疫缺陷疾病,癌症患者最忌讳的就是降低免疫力,这很容易引起癌细胞的反扑。
所幸,日本科学家本庶佑发现了另一个重要的暗号:PD-1。
PD-1是当前医学界大热的研究点,原因有二:第一,正常细胞不太喜欢用这个暗号;第二,癌细胞特别喜欢用这个暗号。
这还有啥好说的,2014年FDA批准了两个新药,欧狄沃和可瑞达,专门破坏T细胞上的PD-1蛋白,可以用来治疗:黑色素瘤、非小细胞肺癌、结直肠癌、肾癌、肝癌、胃癌……
一种药可以治疗这么多癌症,也就电线杆上的广告才敢说。不过PD-1的广告可不是贴在电线杆上的,而是美国前总统卡特的背书。

2015年8月,90岁高龄的美国前总统卡特诊断出黑色素瘤,这是一种恶性程度极高的癌症,晚期的五年生存率只有5%!90岁的高龄无法化疗,而且癌细胞已经扩散到肝脏和大脑,这情况,就是大罗神仙下凡,也只能准备后事了。
但奇迹就这么发生了,可瑞达治疗仅仅4个月后,卡特体内的肿瘤彻底消失了!现在已经过去了4年半,卡特依然活奔乱跳,最近有消息说,94岁的卡特和朋友们去猎火鸡而摔断了臀骨……癌症估计是痊愈了。
当然,不是每个人都像卡特这么幸运,晚期恶性黑色素瘤患者经过PD-1抑制剂治疗后,五年生存率只是提高到了30%-40%,而且有少部分患者出现了不同程度的免疫性炎症。因为很多用PD-1暗号的正常细胞也被T细胞杀死了,甚至还有万分之六的概率导致免疫性心肌炎,这是一种死亡率极高的疾病。

科学家又仔细研究了癌细胞对暗号的过程,发现癌细胞是产生了一种叫PD-L1的蛋白去结合T细胞上的PD-1蛋白,也就是说,癌细胞是用PD-L1蛋白对的暗号,这下就好办了。
2016年FDA批准了第一款PD-L1抑制剂,其原理是结合癌细胞的PD-L1蛋白,使癌细胞没法对上T细胞的暗号。话说,小盆友能分得清PD-1和PD-L1的区别吧。
截止2018年底FDA批准的PD-1/PD-L1抑制剂已经有6款了。除此之外,2018年12月中国国家药品监督管理局正式批准了国内首个自主研发的PD-1抑制剂,君实生物的拓益。和凯美纳一样,这也是中国医药界一个不小的突破。

PD-1/PD-L1抑制剂可以治疗几十种癌症,就是疗效仍不稳定,很多时候T细胞面对癌细胞还是有点发懵,可一旦有效基本就是治愈!本僧得强调一遍,一旦有效就是治愈,这是传统化疗药无法比拟的优势!
更重要的是,与癌症的这场战争中,人类终于看到了胜利的曙光,虽然只是曙光。
第二个补丁
科学家除了对“能对暗号的癌细胞”穷追猛打,对“不放信号的癌细胞”也没有手软。
这类癌细胞因为不发出MHC信号而躲过了免疫系统的检查,于是,科学家就把免疫细胞提取出来,直接人为加上一套新的识别系统,使其能找到不放MHC信号的隐藏癌细胞,这就是:嵌合抗原受体T细胞免疫疗法,简称CAR-T。
美国小女孩Emily是全球第一个试验CAR-T疗法的儿童,这也让CAR-T名声大噪。
2012年6岁的Emily在急性淋巴性白血病两次复发后,已是回天无术,濒临死亡。宾夕法尼亚大学的科学家在征求家人同意后,死马当活马医,采用了当时并未被批准的CAR-T疗法。
他们在癌细胞表面发现了一个特殊的蛋白:CD19蛋白,于是科学家提取了Emily的免疫细胞后,加上了一套能识别CD19蛋白的系统,体外培养增殖后,再重新注入体内。
然后,重回体内的T细胞开始疯狂攻击任何带有CD19蛋白的细胞,激烈的战斗使Emily身体状况更加危急,靠着呼吸机熬过了2周。
随后医生给艾米丽使用了免疫抑制药物,终于让发狂的T细胞冷静了下来。仅仅几个小时,Emily的情况迅速好转,在第二天的7岁生日时醒了过来。再一检查,体内的癌细胞已经完全消失。
直到现在,癌症一直没有复发,Emily每年都会拿着一块“cancer free”的牌子来纪念这个奇迹。

2017年FDA正式批准了首个CAR-T疗法。
CAR-T疗法斩获虽丰,但癌细胞还是顶住了攻势,因为像CD19蛋白这样的靶点并不好找。Emily的癌症是淋巴B细胞癌变引起的,而人体细胞只有淋巴B细胞才有CD19蛋白,所以科学家才会把CD19蛋白作为靶点。可这样会误伤正常的淋巴B细胞,所以Emily必须要注射免疫球蛋白来维持免疫力。
CAR-T疗法对淋巴B细胞引起的急性淋巴细胞白血病和非霍奇金淋巴瘤比较显著,还有一些不太成熟的研究:以ERRB2为靶点治疗肺癌,以前列腺特异性抗原为靶点治疗前列腺癌,以CAIX为靶点治疗肾癌,以Lewis Y为靶点治疗卵巢癌,等等,要走的路还很长。
CAR-T目前无法为人类取得彻底胜利。
再打第二个补丁
顽强的科学家再次发动了新一轮攻势。
癌细胞其实有很多异常蛋白,这些蛋白若是单独出现,早就被免疫系统收拾干净了,正如进入体内的感冒病毒。但是因为有癌细胞的庇护,这些异常蛋白的MHC信号被屏蔽了。
这一轮进攻重点是:解除癌细胞的屏蔽。
科学家把癌细胞提取出来后,找出那些异常蛋白,然后人工合成,再把这些裸露的异常蛋白注入体内。这个工作极其复杂,复杂到本僧都不想多说。
这些异常蛋白大摇大摆进入体内,没了癌细胞庇护,自然不可能躲过免疫系统的侦查,很快蛋白特征就汇报给了总部。接着,T细胞大军出征,攻击任何带有这种蛋白特征的入侵者。于是,一脸懵逼的癌细胞就糟了池鱼之殃。
这过程和疫苗原理有几分类似,被称为“个性化癌症疫苗”,但其实这不算疫苗。
美国波士顿达纳-法伯癌症研究所和德国缅因兹大学,首次在临床试验中使用癌症疫苗治疗取得成功,两组团队的研究成果同时发表在2017年7月的《自然》上。

一共有19位黑色素瘤患者参与试验,美国科学家为每位患者找到了20多种异常蛋白,德国科学家则找到了10多种异常蛋白,将这些蛋白重新注入人体后,激发了T细胞的强烈应答。
19位患者中,12人肿瘤完全消失且无复发,3人在接受辅助治疗后肿瘤也完全消失,1人肿瘤明显缩小,还有3人实在是病情过于严重。
这无疑让人类战胜癌症的曙光又多了几分。
攻守之势异也
癌细胞和免疫系统的对抗很像是电子对抗,双方都在破解对方的密码。
靶向药是我们破解了癌细胞的密码,所以癌细胞只要更改密码就会产生耐药性,搞得我们很被动。
免疫疗法则刚好相反,癌细胞破了免疫系统的密码才发展成癌症,当我们更改了免疫系统的密码,T细胞又重新杀得癌细胞丢盔弃甲。
不过,就是太贵了,听说五百万级别......
最新战况
人类对癌症的第一波总攻可谓气势汹汹,攻城掠地,战功硕硕,但殊死搏斗的癌细胞也爆发出了惊人战力。
2019年3月《自然》杂志为我们呈现了最新战况。在美国小女孩Emily身上创造奇迹的CAR-T细胞免疫疗法遭遇了有史以来最激烈的反扑,复发案例屡见不鲜。
你绝对想不到,狡猾的癌细胞将CD19蛋白这个靶点转移到了T细胞身上,使得T细胞自相残杀,直至消耗殆尽,残存的癌细胞趁机再度壮大。

现在,科学家又在谋划新一轮的反攻方案。加州大学已经从免疫系统里又找到了一位战力爆表的盟友:自然杀伤细胞。这哥们儿已经展现出比T细胞还要强大的潜力,很可能是下一次进攻的主力之一。
战略相持
无论悲观者把癌症描绘得多恐怖,也无论乐观者把免疫疗法说得多神奇,本僧个人以为,人类与癌症的这场战争至少是进入战略相持阶段了,人类虽然收复了很多阵地,但依然有不少啃不动的硬骨头。
本文特意加了很多时间点,仔细看看这些时间点,我们可以明显感受到人类对抗癌症时那种蓬勃向上的气象!
为什么我总是呼吁大家热爱科学,今天总算找到了最硬的理由:将来有一天,当我们遭遇癌症的时候,你就会从心底里期盼,期盼科技能发展得再快一点!也许多活一天,就能听到人类反攻的号角:死神,再见!